摩尔比法(mole ratio method)
若M与R均不干扰MR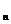 的吸收,且其分析浓度分别是
的吸收,且其分析浓度分别是 、
、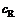 ,那么固定金属离子M的浓度,改变配位体R的浓度,可得到一系列
,那么固定金属离子M的浓度,改变配位体R的浓度,可得到一系列 /
/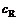 不同的溶液。在适宜波长下测定各溶液的吸光度,然后以吸光度
不同的溶液。在适宜波长下测定各溶液的吸光度,然后以吸光度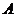 对
对 /
/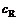 图。
图。
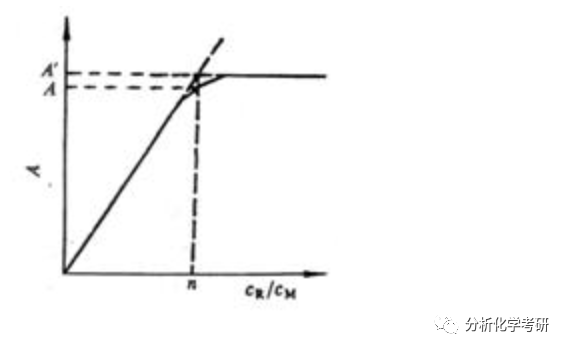
当加入的配位体R还没有使M定量转化为MR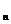 并稍有了过量时,曲线便出现转折;加入的R继续过量,曲线便成水平直线。
并稍有了过量时,曲线便出现转折;加入的R继续过量,曲线便成水平直线。
转折点所对应的摩尔比数便是络合物的组成比。
若络合物较稳定,则转折点明显;反之,则不明显,这时可用外推法求得两直线的交点。交点对应的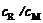 即是
即是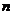 。
。
等摩尔系列法(equimolar series method)
设cM和cR分别为溶液中M与R物质的量浓度,配制一系列溶液,保持cM +cR=c(c恒定)。改变cM和cR的相对比值MRn,在的最大吸收波长下测定各溶液的吸光度A。
当A达到最大时,即浓度MRn最大,该溶液中cM/cR比值即为络合物的组合比。如以吸光度A为纵坐标值cM/c为横坐标作图,即绘出等摩尔系列法曲线。
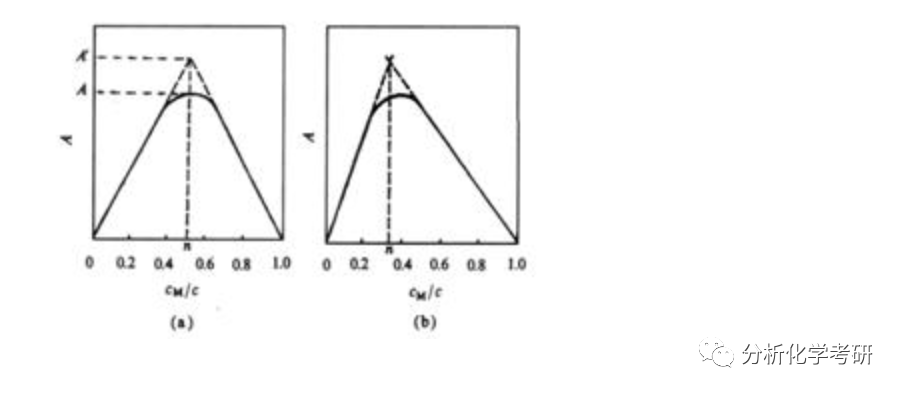
该法适用于溶液中只形成一种离解度小的、配合比低的络合物组成的测定。

- End -
