2025年12月11日,国家药品监督管理局医疗器械标准管理中心(以下简称“标管中心”)发布了《2025年第四次医疗器械产品分类界定结果汇总》,在“建议按照药械组合产品判定程序界定管理属性的产品(35个)”中,首次把透明质酸钠外泌体膜液体敷料明确为“药械组合产品”。这标志着,除已此前公布的先进治疗药品(ATMP)赛道外,外泌体正式拥有了第二条合规产业化路径——药械组合。
外泌体作为当今最前沿的新型生物材料,无论是科研应用还是监管都处于不断的摸索之中。2024年10月,标管中心在《2024年第二次医疗器械产品分类界定结果汇总》中明确干细胞外泌体不作为医疗器械管理,这为外泌体的应用带来了很大限制。
2025年6月,CDE《先进治疗药品的范围、归类和释义(征求意见稿)》首次将细胞外囊泡(含外泌体)纳入ATMP,宣告其药品身份。此次,标管中心将含外泌体膜组分的液体敷料被界定为“以医疗器械为主的药械组合产品”,至此,外泌体药品与器械双通道监管框架正式成型。
外泌体是细胞外囊泡(EVs)中的一类,一般直径大小在30-150nm,人体中几乎所有类型的细胞都能产生外泌体,它广泛存在于组织细胞间隙及体液中。
外泌体发挥生物学效应的主要机制包括三个方面:
通过外泌体表面蛋白或者有生物活性的脂质配体与受体细胞的表面受体结合,实现信号转导;
受体细胞通过内吞作用将外泌体吸收,外泌体进入细胞内后再释放内容物,实现对受体细胞的调控;
外泌体与受体细胞的细胞膜直接融合,并将携带的内容物(mRNA、miRNA、蛋白质等)直接导入受体细胞,实现受体细胞的调控。
这三种机制决定了外泌体在医疗领域的三种主要应用:疾病诊断、治疗和药物递送。
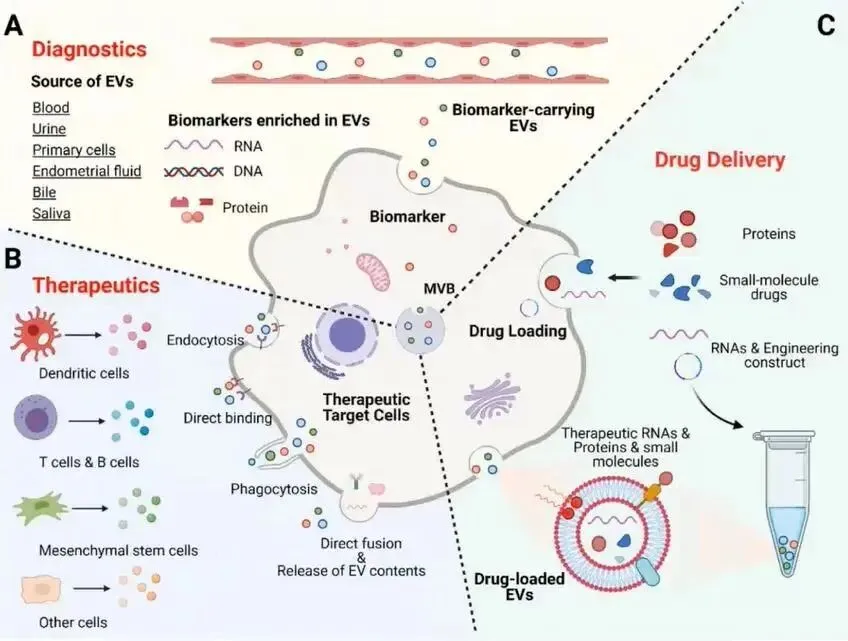
也正因为外泌体三种生物学效应机制同时存在,因此在监管中,难以将其单独列为“医疗器械”进行管理,就此,“药械组合”这种创新的特殊通道应运而生。
透明质酸钠外泌体膜液体敷料作为本次列入“按照药械组合产品判定程序界定管理”唯一一款外泌体产品,充分反应了对外泌体产品作为医疗器械监管的内在逻辑,将外泌体膜作为“物理屏障”,同时考虑到外泌体膜可能发挥促进伤口血管的再生、加速皮肤深度伤口的愈合,抑制炎症反应等生物学活性作用。

因此,药械组合这种模式,无疑为推进外泌体合规应用的一项创举!
值得注意的是,发文中提到的“外泌体膜”并不等同于“外泌体”,而只是基于外泌体“加工”而成的一项“原料”,但目前没有明确的标准来划分二者之间的边界,下一步需制定和发布外泌体膜术语及技术要求的明确标准。
同时,药品与器械双通道监管的成型,也意味着外泌体必须满足药物质量控制及临床前研究指导原则等GMP级要求,这实际本质上对外泌体应用门槛的提高,无论是生物医药企业还是高校、科研院所,在外泌体相关的科研与产品研发中,对外泌体制备的工艺要求将向监管要求对齐,更为先进的三维智造工艺将成为主流快速发展。
从长期来看,外泌体药品与器械双通道监管、药械组合产品管理的模式,更为三维智造外泌体修筑了一条高速公路。三维培养制备的外泌体一改传统二维培养过程模糊质控难、手工操作误差大成本高、空间利用率低产量低、开放性操作易污染、反复酶消化活性差等难题,三维工艺制备的外泌体更均质、更高纯度、单细胞分泌量更高,是让外泌体相关产品符合相关监管要求的重要保证,可以预见,越来越多的外泌体相关产业的机构、企业将采用外泌体三维智造工艺。
免责声明:部分内容来源于网络,版权归原作者所有。本文为科普性知识,仅作信息交流之目的,不做商业用途,如涉及作品内容、版权和其它问题,请联系我们删除。