信熹研究 | 解码免疫风暴——过敏性行业研究
- 2026-06-01 17:56:53
本期信熹研究探讨过敏性疾病从基础机制到前沿疗法的系统性突破。报告首先剖析过敏的生物学核心,揭示Th2型炎症风暴及其上游“警报素”的关键驱动作用;进而梳理药物研发进展,从传统疗法到针对IgE、IL-4/IL-13、IL-5、TSLP等靶点的精准治疗,以及JAK、BTK抑制剂等新型干预策略;同时评估脱敏治疗(AIT)的临床路径与管理方案;最后展望以多靶点抑制剂、细胞耗竭技术和免疫记忆重置为代表的新一代治疗范式。
一、过敏的生物学机制
要理解药物研发的逻辑,必须先看懂过敏反应的微观战场。过敏并非单一症状,而是一场由多细胞、多因子参与的级联反应。
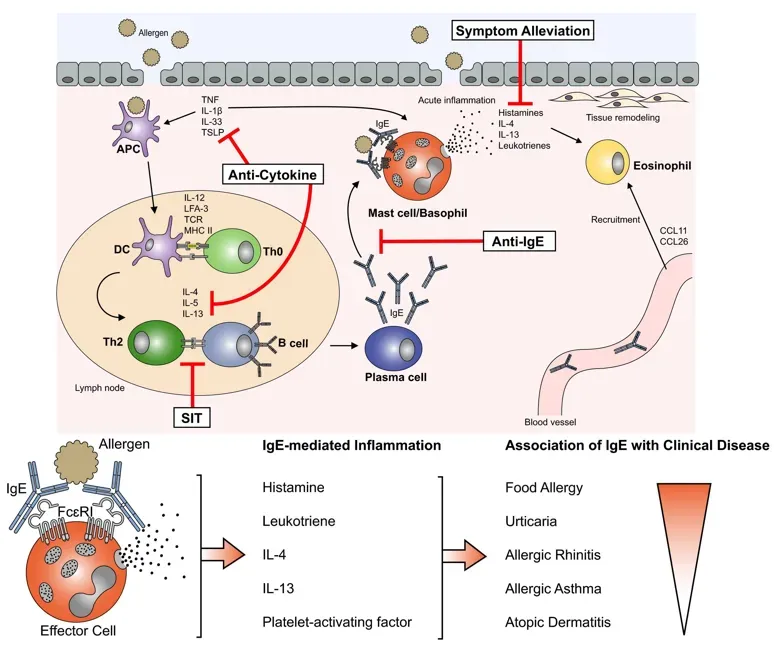
图1 | 过敏反应机制
(来源:网络)
1.1 | 核心轴线:Th2型炎症风暴
过敏的本质是免疫系统对无害物质(过敏原)产生的过度反应,其核心驱动力是Th2(辅助性T细胞2型)通路的异常激活。
启动阶段(致敏):当过敏原(如花粉蛋白、尘螨)突破上皮屏障,抗原呈递细胞(DC细胞)将其摄取并呈递给初始T细胞。在IL-4等微环境诱导下,初始T细胞分化为Th2细胞。
指挥阶段:活化的Th2细胞分泌核心细胞因子——IL-4、IL-5、IL-13。这三者被称为“过敏三剑客”:IL-4 & IL-13:诱导B细胞发生免疫球蛋白类别转换分化为浆细胞,从产生IgG转为产生IgE;同时破坏皮肤屏障功能(下调丝聚蛋白表达),导致“越痒越抓,越抓越漏”的恶性循环,IL-5:专门负责嗜酸性粒细胞(Eosinophils)的成熟、存活和募集。
效应阶段:IgE抗体结合在肥大细胞(Mast Cells)表面的高亲和力受体(FcεRI)上。当再次接触过敏原时,过敏原交联IgE,导致肥大细胞瞬间“爆炸”(脱颗粒),释放组胺、白三烯、前列腺素等介质,引发红肿、瘙痒、支气管收缩等急性症状。
活化的肥大细胞、嗜碱性粒细胞或嗜酸性粒细胞释放的生物活性介质在介导过敏反应中发挥不同的生物学效应。
组胺:是一种小分子量的血管活性胺。组胺通过结合受体,发挥其效应功能。H1~H4等4种组胺受体分布于不同细胞,介导不同的效应。H1介导肠道和支气管平滑肌的收缩、小静脉通透性增加和杯状细胞黏液分泌增多;H2介导血管扩张和通透性增强,刺激外分泌腺的分泌。肥大细胞和嗜碱性粒细胞上的H2则发挥负反馈调节作用,抑制脱颗粒。肥大细胞上H4具有趋化作用。
细胞因子:IL-4、IL-13、IL-33在后期产生,可诱导并放大Th2应答,产生IL-4和IL-13促进B细胞产生IgE;lL-3 、IL-5、GM-CSF促嗜酸性粒细胞分化与活化;TNF-α参与全身过敏反应性炎症,增加血管内皮细胞黏附分子表达。嗜酸性粒细胞、嗜碱性粒细胞和Th2细胞表达CCR3,与嗜酸性粒细胞趋化因子(ECF)结合,趋化和活化嗜酸性粒细胞,对嗜碱性粒细胞、Th2、单核-巨噬细胞和中性粒细胞也具有趋化作用。
脂类介质:前列腺素D2(PGD2)和白三烯C4、D4、E4(LTC4、LTD4、LTE4)与平滑肌细胞和白细胞上的受体结合,促平滑肌收缩;白三烯使支气管平滑肌强烈而持久地收缩,也可使毛细血管扩张、通透性增加和黏膜腺体分泌增加。血小板活化因子(platelet activating factor, PAF)主要参与迟发相反应,使支气管平滑肌收缩,趋化和活化中性粒细胞、嗜酸性粒细胞和血小板等。
酶类:蛋白酶切割纤维蛋白原、活化胶原酶引起组织损伤。糜蛋白酶可引起短暂的血管收缩、减少上皮基底液的分泌。组织蛋白酶G、羧肽酶和嗜酸性粒细胞胶原酶参与结缔组织基质的重塑。嗜酸性粒细胞过氧化物酶可刺激组胺释放。
其他:嗜酸性粒细胞阳离子蛋白和嗜酸性粒细胞衍生的神经毒素具有神经毒性。主要碱性蛋白有刺激肥大细胞和嗜碱性粒细胞活化脱颗粒作用,此效应可被IL-3、IL-5和CM-CSF等增强。
1.2 | 上游开关:上皮来源的“警报素”(Alarmins)
近年来的重大发现是,Th2反应并非起点。受损的上皮细胞(皮肤、气道黏膜)会率先释放一组细胞因子:TSLP(胸腺基质淋巴细胞生成素)、IL-33、IL-25。
它们被称为“警报素”,位于炎症级联反应的最顶端。它们可以直接激活先天淋巴细胞(ILC2),不依赖特异性抗原即可启动2型炎症。这解释了为什么有些哮喘患者IgE不高,但依然有过敏症状(非特应性哮喘)。阻断这一层级,意味着关掉了过敏反应的总水闸。
临床上,过敏往往遵循“特应性皮炎(婴儿期) -> 食物过敏 -> 过敏性鼻炎 -> 哮喘(儿童/成人)”的演变规律。
药物研发不再满足于治疗单一适应症,而是追求“异病同治”。例如,针对IL-4Rα的药物之所以能通吃皮炎、哮喘和鼻息肉,正是因为它阻断了贯穿整个过敏进程的核心通路。
二、过敏药物的开发
1、传统过敏药物
在过去的几十年里,过敏治疗主要依赖“老三样”:抗组胺药、糖皮质激素、白三烯受体拮抗剂。虽然它们是基础用药,但在面对中重度、复杂性过敏时,局限性日益凸显。
表1 | 过敏药物分类
(来源:信熹资本整理)
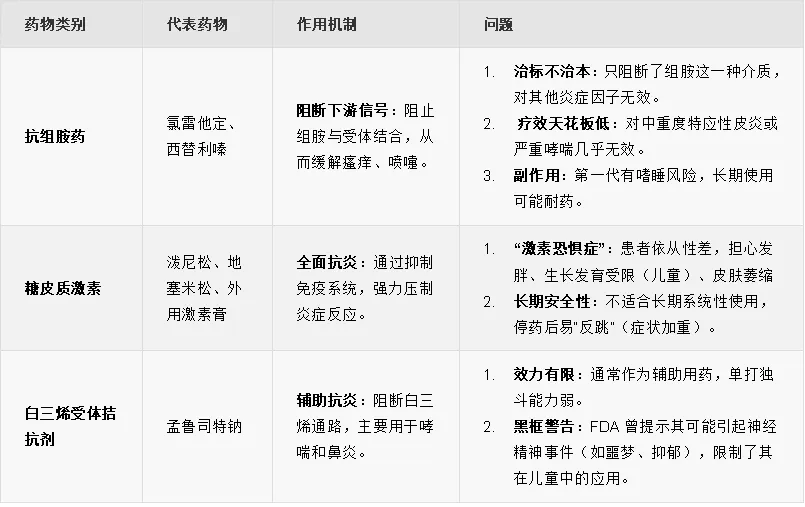
传统疗法的最大痛点在于——它们要么是“撒胡椒面”式的全面压制(激素),副作用大;要么是“只堵枪眼”式的末端阻断(抗组胺),效果不彻底。
2、新机制与新药物:精准打击2型炎症风暴
近年来的生物学突破发现,大多数过敏反应(特应性皮炎、哮喘、食物过敏)的核心驱动力是 “2型炎症通路”(Type 2 Inflammation)。新的药物研发思路不再是去堵下游的组胺,而是逆流而上,去阻断上游的“指挥官”细胞因子。核心的机制突破包括三大关键靶点:
IgE(免疫球蛋白E):过敏反应的“扳机”。它结合在肥大细胞表面,一旦遇到过敏原,就扣动扳机引发爆炸(脱颗粒)。
IL-4 / IL-13(白介素4/13):2型炎症的“总司令”。它们指挥B细胞生产IgE,破坏皮肤屏障,引发瘙痒。
TSLP / IL-33(上皮细胞因子):炎症的“警报器”。位于皮肤和黏膜最上层,一受到刺激就拉响警报,启动整个级联反应。
2.1 | 抗IgE通路
Omalizumab(奥马珠单抗):结合游离IgE的Cε3结构域,阻断其与肥大细胞FcεRI受体的结合。注意,它不结合已结合在细胞表面的IgE,因此不会诱发过敏。2024年获批用于食物过敏的脱敏辅助治疗。技术逻辑是提高患者的过敏阈值,防止意外摄入导致的休克,而非治愈。
下一代高亲和力抗体(Ligelizumab):具有比奥马珠单抗高几十倍的亲和力,尽管亲和力高,但在慢性自发性荨麻疹的III期临床中未能表现出显著优于奥马珠单抗的疗效。这给业界的启示是:单纯提高亲和力可能触到了生物学效应的天花板,机制创新比参数优化更重要。
2.2 | 抗IL-4/IL-13通路:Th2的“双重封锁”
IL-4和IL-13是免疫系统中的关键的T辅助细胞2型(Th2)细胞因子,在2型炎症反应(如过敏、哮喘)中起核心作用,它们共享一个共同的受体链(IL-4Rα),因此可以同时被靶向,成为治疗自身免疫病和过敏性疾病的重要药物靶点,通过抑制它们的共同信号通路,来阻断炎症级联反应。
Dupilumab(度普利尤单抗):
度普利尤单抗是目前过敏领域的“药王”,2024年销售收入142亿美金,并且仍在不断攀升。从机制上来看,度普利尤单抗不结合IL-4或IL-13配体,而是结合IL-4Rα受体亚基。由于IL-4和IL-13信号传导都需要共用这个受体亚基,因此Dupilumab实现了“一石二鸟”,同时阻断了两个核心细胞因子。通过阻断IL-4和IL-13,它能有效控制这些炎症因子在特应性疾病(如过敏性皮炎、哮喘)中的病理作用。从特应性皮炎到哮喘,再到结节性痒疹、嗜酸性食管炎,其广谱性源于对Th2核心通路的精准卡位。适应症的拓展也不断提高度普利尤的天花板。
IL-13单靶点药物(Lebrikizumab, Tralokinumab):
竞争策略: 理论上保留IL-4的功能可能对维持某些免疫防御有益,但在疗效上,目前尚未证明显著优于双靶点阻断。它们更多是在给药频率(如更长效)上寻找差异化。
2.3 | 抗IL-5通路:嗜酸性粒细胞的“定点清除”
IL-5 可诱导嗜酸性粒细胞的成熟、激活和募集,引发由嗜酸性粒细胞造成的过敏性疾病。 针对 IL-5 或者其受体 IL-5R,已有多款新药获批。优时比的瑞利珠单抗(IL-5)于 2016 年 3 月获批上市,用于治疗嗜酸性粒细胞哮喘(EA),针对哮喘适应症已进入 III 期临床; GSK 的美泊利珠单抗(IL-5)已获批CRSwNP、 EA、EGPA、哮喘 4 个适应症。阿斯利康的 Benralizumab 已获批 EA 与哮喘 2 个适应症,其针对CRSwNP 适应症已申报 NDA。
Mepolizumab / Reslizumab:直接结合IL-5配体,阻止其与受体结合。相当于切断了嗜酸性粒细胞的“粮草”。
Benralizumab(本瑞利珠单抗):直接结合嗜酸性粒细胞表面的IL-5Rα受体。其Fc段经过岩藻糖基化修饰(Afucosylation),极大增强了与NK细胞CD16的结合力,诱导NK细胞直接杀伤嗜酸性粒细胞。这不仅是阻断信号,更是物理清除细胞,起效更快、更彻底。
2.4 | 上游TSLP通路:广谱的“截流闸”
Tezepelumab:作用于上皮细胞来源的TSLP,是唯一不局限于Th2高表达人群的哮喘生物制剂。对于那些嗜酸性粒细胞不高、IgE也不高的“低Th2型”哮喘患者,Tezepelumab提供了唯一的生物药选择。这标志着过敏治疗从“表型驱动”向“内型(Endotype)驱动”的跨越。
上述生物制剂在不同的领域内有各自的优势,但在给药方式上较为复杂,因此产业界也从未放弃对小分子的研发,小分子药物的研发重点在于“外用制剂技术”和“激酶选择性”。
2.5 | JAK抑制剂:细胞内的信号截断
JAK-STAT是细胞因子受体下游的关键信号通路。虽然 JAK 抑制剂覆盖了多个自免适应症领域,但在过敏疾病领域主要针对特应性皮炎(AD)进行布局。因此相较于口服JAK抑制剂安全性堪忧,外用制剂在这个领域有明显优势,但外用制剂既要保证药物穿透角质层进入真皮,又要防止药物大量吸收入血产生全身副作用(如血栓、感染风险),这需要极高的制剂工艺。目前获批的JAK外用制剂仅有Ruxolitinib。
2.6 | BTK抑制剂:肥大细胞的“静音键”
机制迁移:BTK不仅在B细胞中表达,也是肥大细胞FcεRI信号传导的关键激酶。直接抑制肥大细胞和B细胞内部的布鲁顿氏酪氨酸激酶(BTK)可以阻止肥大细胞脱颗粒。
被认为是“慢性荨麻疹”和“食物过敏”的下一个重磅炸弹。它能让肥大细胞“哑火”,不再释放组胺,且没有JAK抑制剂那样的安全性担忧。
三、脱敏治疗(AIT)
过敏原特异性免疫治疗(AIT),俗称脱敏治疗,是在明确患者过敏原后,将过敏原制剂通过逐渐增量、反复给药的方式诱导机体免疫系统产生耐受,遏制过敏性炎症进展,从而改善患者症状。AIT是目前唯一可能改变过敏性疾病自然进程的对因疗法,兼具治疗和预防(例如可减少过敏性鼻炎发展为哮喘)双重意义。该疗法的有效性和安全性获国际认可,具备长期获益甚至达到临床治愈的效果。
3.1 | 患者是否适合AIT
AIT成功的第一要素是“天时”,即患者是否适合AIT,实现精准患者选择是AIT首要关键。过敏原皮肤点刺试验(SPT)和血清特异性免疫球蛋白(Ig)E检测是筛选适合AIT患者的主要依据。然而,许多患者由于多重过敏反应或由于交叉反应物的存在而对多种过敏原致敏,这会阻碍对过敏原来源的识别、影响精准诊治。过敏原组分诊断(CRD)是通过天然纯化或重组表达的过敏原组分蛋白来识别引起过敏的特定组分的一种精准诊断技术,可避免过敏原粗提物非致敏成分的干扰,从而更好地将致敏与治疗相匹配,在优化过敏原规避方案和开展准确的AIT方面发挥重要作用。同时,CRD还有助于判断疾病严重程度、预测哮喘发生风险,从而可将患者进一步分层,预警潜在的治疗风险,提升AIT的安全性。近年来,CRD愈加趋向于集成化、自动化和国产化,目前国内外常用的检测方法包括荧光免疫法、免疫固相过敏原芯片法、蛋白芯片法、纳米磁微粒化学发光免疫分析法以及免疫捕获法等。
3.2 | 治疗方案选择
AIT成功的第二要素是“地利”,即治疗方案能否起效。目前AIT的给药途径和方案正不断优化,皮下免疫治疗(SCIT)和舌下免疫治疗(SLIT)两种主流免疫疗法的疗效得到越来越多强有力的证据支撑。新兴给药途径展现出巨大潜力,过敏原淋巴结内注射免疫治疗通过超声引导直接注射至淋巴结,产生免疫应答,目前治疗过敏性鼻炎的临床研究多采用3次注射,总疗程2个月,短期疗效与SCIT相当且安全性良好。表皮免疫治疗采用贴片形式,在牛奶、花生等食物过敏中显示出良好的有效性和安全性。皮内、鼻内及口服等途径也在探索中。在给药方案方面,常规AIT需3年疗程,而加速免疫治疗方案作为一种缩短AIT剂量累积阶段的创新方法,能更快地达到维持剂量阶段,从而减少患者的就诊次数和治疗时间,主要包括集群治疗和冲击治疗等多种形式。目前,加速免疫治疗在提高疗效和患者便利性方面具有明显优势,但其长期安全性和适用范围仍在进一步研究和优化。
过敏原制剂(也称过敏原疫苗)的质量直接影响AIT的疗效。理想的制剂应具备含量稳定、纯度高、特异性强的特点,以诱导安全持久的免疫应答。传统制剂采用天然过敏原提取物,虽经标准化处理,但仍存在纯度和稳定性不足的问题。随着生物技术的进步,新型制剂研发聚焦两个方向:一是应用新型佐剂(如脂质体、Toll样受体(TLR)激动剂等),通过纳米技术增强靶向递送和免疫原性;二是采用基因工程技术改造过敏原结构,包括重组过敏原和合成肽段疫苗。这些新型制剂具有纯度高、稳定性好、易于生产等优势,但尚需更多大样本和高质量的临床试验证据。
3.3 | 患者的长期管理
AIT成功的第三要素为“人和”,即能否实现患者长期安全有效的管理。数字化医疗技术正在革新过敏性疾病的管理模式。移动健康技术通过短信、电话、自动语音应答、移动应用程序等多种形式,为过敏患者提供全方位的疾病管理支持。例如,全球应用的“移动气道监测网(MASK)”平台,作为一款智能化的过敏日记系统,已在23个国家和地区投入使用,帮助患者记录日常症状、用药情况及过敏原暴露信息,并定期评估疾病对生活质量的影响。在中国,基于应用程序(APP)和微信小程序的移动医疗解决方案快速发展,涵盖症状监测、复诊提醒和远程随访等功能,显著提升了AIT的依从性和疗效。值得注意的是,在推进数字化管理的同时,必须高度重视患者数据安全和隐私保护。展望未来,将临床决策支持系统与移动平台深度整合,有望实现更精准的患者分层管理、个性化治疗方案制定和智能化治疗决策,同时通过高质量的健康教育和自我管理指导,帮助患者建立长期有效的疾病控制机制。这一发展趋势不仅为患者带来更高效、个性化的治疗选择,也标志着AIT正向着更精准、安全和便捷的方向持续进步。
四、新机制与新靶点的突围
针对Dupilumab等现有药物无效的“难治性”患者,研发正向更底层的细胞生物学机制迈进。
4.1 | 新型三功能抑制剂
Excellergy由Red Tree Venture Capital于2021年创立,总部位于加利福尼亚州帕洛阿尔托,正在开拓一种新的治疗类别,旨在完全控制过敏性疾病。基于斯坦福大学Ted Jardetzky教授和瑞士伯尔尼大学Alexander Eggel教授在IgE与其受体结构结合方面的科学进展,该公司开发了一系列三功能ECRI,这些ECRI利用了成熟的IgE药理学,同时超越了目前的限制,目标是重新定义多种过敏性疾病的标准疗法。
这类新的ECRI采用了一种三功能作用机制:(1)快速去除肥大细胞和嗜碱性粒细胞上与FceRI结合的IgE,而不会触发这些细胞的激活;(2)提供有效的、高亲和力的游离IgE中和;(3)加速FceRI表达的下调。与现有的批准治疗相比,这三种功能同步作用,有可能在更广泛的患者群体中实现更快的起效和更完全的过敏控制。
4.2 | 细胞耗竭技术:物理清除致病细胞
KIT (CD117) 抑制剂,KIT受体是肥大细胞生存的绝对依赖因子。抗KIT单抗不仅抑制其活化,更能导致组织驻留型肥大细胞的凋亡和耗竭。在慢性诱导性荨麻疹的临床数据中,Barzolvolimab展现出了惊人的完全缓解率。这证明了“细胞耗竭”策略在过敏领域的巨大潜力。
Barzolvolimab是一种靶向肥大细胞上 c-KIT 受体的单克隆抗体,能有效耗竭肥大细胞群。相较于仅阻断下游介质的前代药物,这是一种全新的治疗策略。在Barzolvolimab的二期临床实验中,与安慰剂组相比,150 毫克和 300 毫克剂量组的 UAS7 评分均显著降低。 值得注意的是,至第 12 周时,150 毫克组和 300 毫克组分别有 38%和 51%的患者达到完全缓解(UAS7 评分=0)。超过 35%的患者在最后一次给药后 28 周仍维持完全缓解状态,这凸显了巴佐伏利单抗潜在的疾病修饰效应。在安全性方面,同样表现良好,在第 76 周时,40%至 48%的患者皮肤病生活质量指数评分低于 1 分,表明该药物未对生活质量造成影响。 睡眠质量、焦虑及压力水平均有改善,有效减轻了阵发性荨麻疹的整体负担。该药物在未接受奥马珠单抗治疗及既往治疗人群中均展现出相当疗效,填补了生物制剂难治性患者治疗领域的重大空白。
Siglec-8 激动剂,Siglec-8是仅表达在嗜酸性粒细胞和肥大细胞表面的抑制性受体。与传统的阻断抗体不同,这是一种激动型抗体(Agonist Antibody)。它结合受体后,会向细胞内传递“死亡信号”,诱导嗜酸性粒细胞凋亡,并抑制肥大细胞脱颗粒。
Siglec-8激动抗体lirentelimab(AK002)是一款非岩藻糖基化的人源化IgG1单克隆抗体,可特异性激活抑制性受体Siglec-8,能够耗竭嗜酸性粒细胞并抑制肥大细胞的活化,从而治疗嗜酸性炎症疾病。
体外和体内研究表明,lirentelimab可以抑制多种肥大细胞活化模式,包括IgE/FcεRI、 IL-33/STL2、Substance P/MRGPRX2和TLR3。人体临床研究中,lirentelimab显著减少血液和组织中的嗜酸性粒细胞。
基于lirentelimab此前在临床前和早期临床的优异数据,以及lirentelimabz治疗嗜酸性胃炎/十二指肠和嗜酸性粒细胞性食管炎(EG/EoD)的失败,Allakos公司对lirentelimab在治疗荨麻疹和特异性皮炎上寄予厚望。除了传统的静脉注射制剂,Allakos公司还开发了lirentelimab的皮下制剂。
2024年1月16日,Allakos宣布核心管线Siglec-8激动抗体lirentelimab在治疗特应性皮炎和慢性自发性荨麻疹的2项关键试验中,均未达到主要终点。
尽管在嗜酸性胃肠炎的临床试验中遭遇波折(症状改善不显著尽管细胞数下降),但这提示我们:组织中的细胞数量减少并不等同于组织功能的完全恢复,可能涉及更复杂的组织修复机制。
4.3 | 免疫检查点干预:重置免疫记忆
OX40/OX40L 通路:OX40是T细胞的共刺激分子。阻断OX40-OX40L相互作用,可以阻止致病性Th2细胞的克隆扩增,并诱导记忆T细胞的凋亡。
Amgen的Rocatinlimab和Sanofi的Amlitelimab均靶向OX40L。作为一种人源化IgG1抗体,Rocatinlimab通过抑制OX40信号通路来减少病理性T细胞,从而重建免疫平衡。ROCKET-IGNITE和ROCKET-HORIZON研究分别在19个国家内进行了为期24周的临床试验,研究对象为近1500名至少患有一年中重度特应性皮炎的成人患者。这些试验纳入了过去对其他疗法无明显应答的患者,反映了更加真实的患者人群状况。试验结果表明,24周后,rocatinlimab组的患者在湿疹面积和严重程度指数(EASI)改善以及总体评估评分上均显著优于安慰剂组。IGNITE研究中,高剂量组和低剂量组的EASI-75应答率分别达到了42%和36%,而安慰剂组仅为13%。而在HORIZON研究中,高剂量组的EASI-75应答率为33%,显著高于安慰剂组的14%。在多项次要终点中,rocatinlimab同样表现出色,包括瘙痒减轻、皮肤疼痛改善及生活质量提升等指标。这说明,该药不仅在主要病症的改善上有显著效果,还在整体生活质量的提升中发挥了积极作用。
与阻断IL-4/13(停药即复发)不同,靶向OX40有望实现“长效缓解”。即在疗程结束后,由于致病性记忆T细胞被清除,患者可能在相当长一段时间内不再复发。这是目前特应性皮炎领域最令人兴奋的“治愈性”探索。
总结来看,过敏药物的开发主要是几个方向:
1. 靶点上移与下潜: 从中游的细胞因子(IL-4/5/13)向更上游的警报素(TSLP/IL-33)和更底层的细胞生存信号(KIT/Siglec-8)扩展。
2. 机制从阻断到清除: 从单纯的中和信号,转向利用ADCC效应或诱导凋亡来物理清除致病细胞,追求更深度的缓解。
3. 治疗目标的升维: 从控制症状(Symptom Control)向疾病修饰(Disease Modification)和免疫重塑(Tolerance Induction)迈进,最终目标是实现“临床治愈”。
五、结语
过敏医药行业正处于一个技术爆发的黄金时代。随着对免疫网络认知的颗粒度不断精细化,未来的药物将不再是千人一面的“广谱抗炎”,而是基于生物标志物(Biomarker)的精准免疫调节。对于研发机构而言,谁能掌握“细胞耗竭”和“免疫重塑”的核心技术,谁就掌握了下一代过敏治疗的王座。
END
延伸阅读
信熹洞见 · 研究
信熹对话
信熹伙伴
北外滩科创会客厅

